Principe de la technique
CAR-T cells signifie cellules T à récepteur antigénique chimérique.
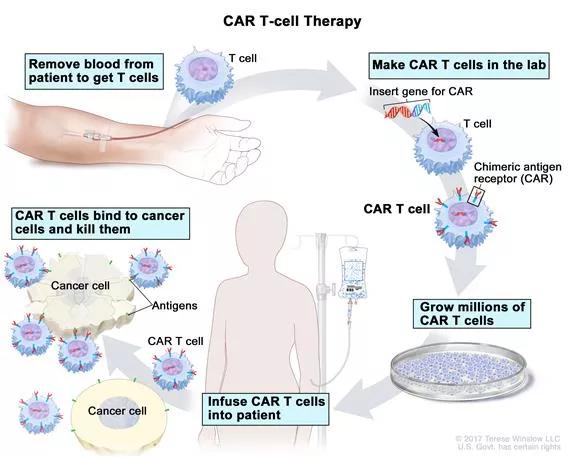
Le principe de cette immunothérapie consiste à modifier génétiquement en laboratoire les lymphocytes T, afin de les munir d’un récepteur (le CAR) qui identifie les cellules cancéreuses et les détruit.
Dans un premier temps, les lymphocytes T du patient sont prélevés par leucaphérèse. Ils sont ensuite envoyés dans un laboratoire spécialisé qui procède à la modification génétique. Les lymphocytes modifiés expriment le nouveau récepteur CAR et se multiplient. Ils sont ensuite réadministrés au patient au cours d’une unique perfusion.

Indications
Les indications thérapeutiques de Kymriah® et Yescarta® sont les suivantes :
- Yescarta® est indiqué dans le lymphome diffus à grandes cellules B et lymphome médiastinal primitif à grandes cellules B réfractaire ou en rechute, après au moins deux lignes de traitement systémique, chez le patient adulte.
- Kymriah® est indiqué chez les enfants et jeunes adultes jusqu’à 25 ans atteints de leucémie aigüe lymphoblastique (LAL) à cellules B réfractaire, en rechute après greffe ou après la deuxième rechute ou plus et chez les adultes atteints de lymphome diffus à grandes cellules B (LDGCB) en rechute ou réfractaire après la deuxième ligne ou plus d’un traitement systémique.
Prise en charge sur la liste en sus
La prise en charge par l'assurance maladie est conditionnée au recueil et à la transmission d'informations relatives à la prescription. Les informations à renseigner sont précisées dans l'arrêté du 20 avril 2019 pour Yescarta® et dans l'arrêté du 20 décembre 2019 pour Kymriah®.
Réglementation
| Arrêté du 8 août 2019 modifiant l'arrêté du 28 mars 2019 | limitant l'utilisation de médicament de thérapie innovante à base de lymphocytes T génétiquement modifiés dits CAR-T Cells autologues indiqués dans le traitement de la leucémie aiguë lymphoblastique à cellules B et/ou du lymphome à grande cellule B, à certains établissements de santé en application des dispositions de l'article L. 1151-1 du code de la santé publique |
| Notice technique n° ATIH-371-6-2019 du 22 juillet 2019 | vise à informer des consignes et du format de recueil des informations relatives à la prescription des traitements de type CAR-T cells pour les établissements de santé concernés |
| Arrêté du 8 juillet 2019 | subordonnant la prise en charge d’un médicament par l’assurance maladie au recueil et à la transmission de certaines informations relatives à sa prescription, en application de l’article L. 162-17-1-2 du code de la sécurité sociale |
| Décret n° 2019-489 du 21 mai 2019 | relatif aux pharmacies à usage intérieur. Il précise les activités comportant des risques particuliers nécessitant une autorisation délivrée pour une durée de 5 ans dont la mise sous forme appropriée des médicaments de thérapie innovante préparés ponctuellement |
| Arrêté du 30 avril 2019 | subordonnant la prise en charge d'un médicament par l'assurance maladie au recueil et à la transmission de certaines informations relatives à sa prescription (Yescarta®), en application de l'article L. 162-17-1-2 du code de la sécurité sociale |
| Arrêté du 20 décembre 2019 | subordonnant la prise en charge d'un médicament par l'assurance maladie au recueil et à la transmission de certaines informations relatives à sa prescription (Kymriah®), en application de l'article L. 162-17-1-2 du code de la sécurité sociale |